유전자 편집 기술과 면역 티세포 결합
16명 중 5명한테서 암 진행 중단 성과
16명 중 5명한테서 암 진행 중단 성과

미 버클리 캘리포니아대(UC버클리) 연구진이 개발한 크리스퍼카스9 유전자 가위(보라색). UC버클리 제공

전자현미경으로 본 티세포. 미 국립보건원 제공
“역대 임상시험 중 가장 복잡한 치료법” 연구팀은 우선 실험에 참가한 각 환자의 혈액과 암 세포를 채취해 종양에는 있지만 혈액에는 없는 돌연변이 단백질을 가려냈다. 돌연변이는 사람마다 다르게 나타나기 때문이다. 연구진은 이어 알고리즘을 이용해 어떤 돌연변이가 면역세포인 티세포의 반응을 유발할 수 있는지 살펴봤다. 그런 다음 일련의 분석 과정을 통해 돌연변이를 인식할 수 있는 티세포 수용체로 불리는 단백질을 만들고, 각 환자의 혈액 샘플을 채취한 뒤 크리스퍼 유전자가위로 이 수용체를 티세포에 주입했다. 크리스퍼 유전자가위는 크리스퍼라는 유전물질(RNA)와 카스라는 효소단백질로 구성된 유전자 편집 도구로, 크리스퍼가 표적 부위로 이동하면 카스가 표적을 절단한다. 마지막으로 연구진은 이 티세포를 배양한 뒤 환자의 혈액에 주입했다. 이 치료법의 설계자인 펜실베이니아대 조지프 프라이에타 교수는 “이 과정은 매우 복잡해서 어떤 환자의 경우엔 1년 이상이 걸렸다”고 말했다. 연구진은 환자별로 표적 물질이 서로 다른 유전자편집 티세포를 최대 3개까지 주입했다. 새 치료법인 만큼 환자의 안전을 위해 양은 적게 했다. 연구진은 이후 이들 티세포가 온몸을 순환하면서 유전자 조작을 하지 않은 티세포보다 종양 주변에 더 많이 포진하는 걸 확인했다. 유전자편집 티세포를 주입하고 한 달이 지나자 전체 실험참가자의 3분의 1인 5명한테서 암세포가 더 이상 자라지 않는 걸 확인했다. 환자 가운데 2명은 고열, 오한 등의 부작용을 보였다. 리바스 교수는 다음번엔 티세포 수를 늘려 실험할 필요가 있다고 말했다.
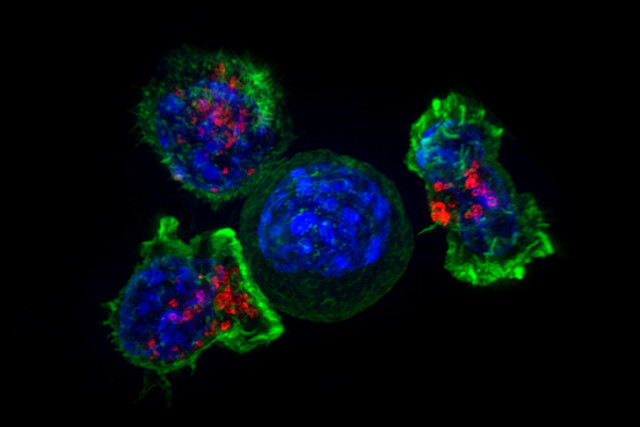
암세포(가운데 파란색)를 둘러싸고 있는 티세포(녹색 및 빨간색). 미 국립보건원 제공
고형암에 맞춤형 유전자요법 기반 닦아 유전자 조작 티세포를 이용한 치료법은 이미 일부 혈액암과 림프암 치료용으로 쓰이고 있다. ‘카 티세포’(키메라 항원 수용체 발현 티세포, chimeric antigen receptor-T)라는 이름의 이 티세포는 환자의 티세포에 암세포에만 반응하는 수용체를 발현시키는 유전자를 삽입한 것이다. 이 티세포는 암세포 표면에 발현되는 단백질에만 작용한다. 이 단백질은 많은 혈액암과 림프암에서 두루 발견된다. 그러나 고형암에는 이 단백질이 없다. 이번에 개발한 치료법은 그런 면에서 맞춤형 티세포 조작이라는 암 유전자요법의 새로운 영역을 개척했다는 의미가 있다. 관건은 물론 성공률을 높이는 것이다. 연구진은 앞으로 유전자편집 티세포의 배양 기간을 단축하는 한편, 주입한 티세포가 암세포에 접근했을 때 더욱 활발하게 활동할 수 있는 방향으로 기술을 개발해갈 계획이다. 암세포는 티세포가 접근해올 경우 면역억제 화학물질을 방출한다. 연구진은 이 면역 억제 신호에 반응하는 티세포 수용체를 제거하면 티세포의 활동력이 더 좋아질 수 있을 것이라고 밝혔다. 곽노필 선임기자 nopil@hani.co.kr
항상 시민과 함께하겠습니다. 한겨레 구독신청 하기







![[사설] 노동자 안전 뒷전 중대재해법 후퇴가 민생 대책인가 [사설] 노동자 안전 뒷전 중대재해법 후퇴가 민생 대책인가](http://flexible.img.hani.co.kr/flexible/normal/300/180/imgdb/child/2024/0116/53_17053980971276_20240116503438.jpg)

![[올해의 책] 숙제를 풀 실마리를 찾아, 다시 책으로 ①국내서 [올해의 책] 숙제를 풀 실마리를 찾아, 다시 책으로 ①국내서](http://flexible.img.hani.co.kr/flexible/normal/800/320/imgdb/original/2023/1228/20231228503768.jpg)
![[올해의 책] 숙제를 풀 실마리를 찾아, 다시 책으로 ②번역서 [올해의 책] 숙제를 풀 실마리를 찾아, 다시 책으로 ②번역서](http://flexible.img.hani.co.kr/flexible/normal/500/300/imgdb/original/2023/1228/20231228503807.jpg)










