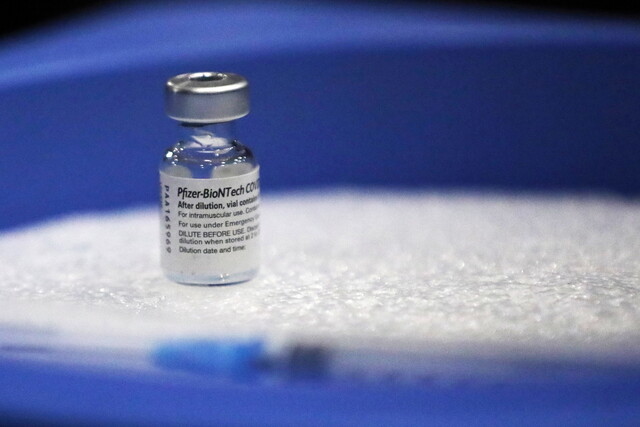
화이자-바이오엔테크의 코로나19 백신. 로이터/연합뉴스
미국 보건당국이 12세 미만 어린이에 대한 화이자의 코로나19 백신 사용을 10월에 승인할 수 있다고 <로이터> 통신이 보도했다.
11일 <로이터>에 따르면, 상황을 잘 아는 두 소식통은 내달 말까지 5∼11세 어린이에게 화이자 코로나19 백신의 사용 승인이 이뤄질 수 있을 것으로 미 고위 보건 당국자들은 생각하고 있다고 말했다.
이 일정은 화이자가 이달 말까지 해당 연령대에 대한 미 식품의약국(FDA)의 긴급사용 승인을 요청하기에 충분한 임상시험 자료를 확보한다는 예상을 기반으로 한다고 소식통은 말했다. 당국자들은 FDA가 화이자의 승인 신청 후 3주 이내에 백신 접종이 어린이에게 안전하고 효과적인지에 대한 결정을 내릴 수 있을 것으로 예상한다고 <로이터>는 전했다.
한 소식통에 따르면 앤서니 파우치 미 국립알레르기·전염병연구소 소장은 전날국립보건원(NIH) 직원들이 참석한 온라인 타운홀 미팅에서 일정의 윤곽을 밝혔다. 파우치 소장은 화이자가 9월 말까지 긴급사용 승인 신청서를 제출하고, 임상 자료가 뒷받침한다면 10월 중하순까지 화이자 제품이 준비될 것 같다고 말했다. 다른 소식통은 FDA가 화이자에 대해 이와 비슷한 일정을 예상했다고 전했다.
파우치 소장은 모더나는 5∼11세 어린이에 대한 자료를 수집하고 분석하는 데 화이자보다 약 3주 정도 더 걸릴 것으로 보인다고 말했다. 모더나에 대한 결정은 11월께 나올 수 있다고 추정했다.
앞서 화이자는 9월에 5∼11세 어린이에 대한 데이터를 준비하고 긴급사용 승인을 신청할 계획이라고 밝혔다고 <로이터>는 전했다. 파우치 소장을 포함한 연방 보건 규제 당국자들은 이전에는 FDA의 결정이 11월이나 그 이후에 나올 수 있을 것이라는 의견을 제시했었다.
<로이터>에 따르면, FDA는 전날 백신 업체들이 자료를 제출하면 어린이를 위한 코로나19 백신을 신속히 승인하기 위해 노력할 것이라고 밝혔다. 긴급사용을 승인하기 위해 더 빠른 경로를 기반으로 신청서를 고려할 것이라고 FDA는 말했다. 이런 긴급승인을 받으려면 회사는 임상시험 참가자에 대한 2개월간의 안전 데이터를 제출해야 하며 완전한 허가에는 6개월이 필요하다고 로이터는 전했다. 연합뉴스