유니스트 조윤경 교수팀, 장기칩 활용해 규명
유방암 세포서 나온 나노소포체가 전이 촉매
유방암 세포서 나온 나노소포체가 전이 촉매
11월24일 발행된 국제학술지 ‘ACS나노’ 표지 사진. 나노소포체(큰 파란색 구)가 간의 미세환경 변화를 일으켜 유방암 세포(초록색)가 간 혈관에 잘 달라붙는 걸 묘사했다.
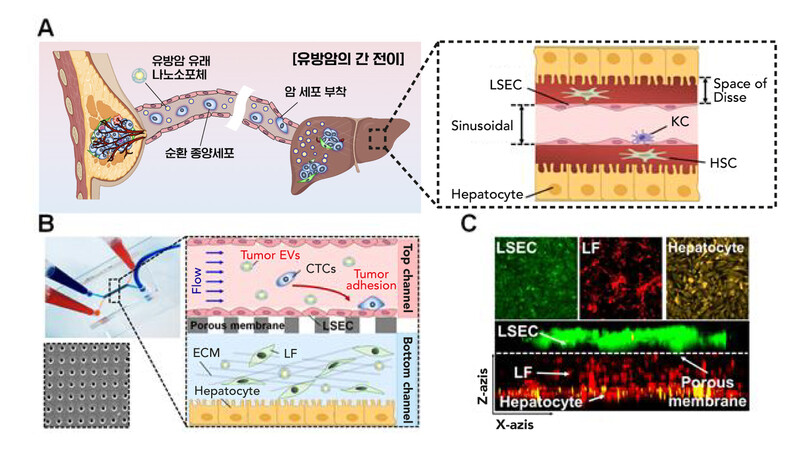
유방암의 간 전이 현상과 간을 모방한 간온어칩(Liver-on-a-Chip) 구조. (A)는 간 전이 과정, (B)는 인간 간온어칩 구조, (C)는 인간 간온어칩의 현미경 이미지. 유니스트 제공
암 전이 ‘토양-씨앗’ 가설 확인…나노소포체가 비료 역할 연구팀은 이번에 간 세포가 배양된 칩을 이용해 이 가설을 검증하는 데 성공했다. 실험 결과 유방암 세포에서 나온 나노소포체는 간의 혈관벽을 더 끈끈하게 함으로써 ‘암 전이의 씨앗’ 역할을 하는 순환종양세포가 혈관벽에 3배 이상 더 잘 달라붙게 만들었다. 나노소포체 표면에 있는 종양성장인자(TGFβ1)가 혈관 벽의 끈끈이 성질을 강화해주는 역할을 한다. 연구진은 대조군 실험을 통해, 간 전이가 발생한 유방암 환자는 간 전이가 안된 유방암 환자나 정상인보다 나노소포체의 종양성장인자 발현양이 많은 것도 확인했다. 조윤경 교수는 “장기에 암 세포가 뿌리내리기 좋은 환경이 조성돼야 전이가 잘 발생한다는 ‘토양과 씨앗’ 가설이 이번 연구로 힘을 얻게 됐다”며 “나노소포체는 이 과정에서 토양을 비옥하게 만드는 ‘비료’ 역할을 하는 셈”이라고 설명했다. `토양-씨앗 가설'이란 암의 전이가 무작위로 일어나는 것이 아니라 원래의 암 부위에서 나오는 순환종양세포(CTCs)와 특정 장기 사이의 상호작용에 의해 호의적인 환경이 조성돼야 생겨난다는 이론이다.
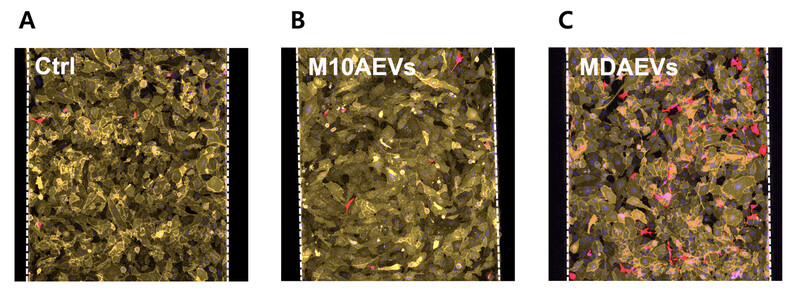
나노소포체에 의해 간 혈관세포에 달라붙는 유방암 세포 양이 증가한 모습(주황색은 간 혈관 세포, 빨간색은 유방암 세포). (A)는 나노 소포체 없는 경우, (B)는 정상 유방세포발 나노소포체를 흘려준 경우, (C)는 유방암 세포발 나노소포체를 흘려준 경우.
췌장암 나노소포체서도 같은 효과 확인 논문 제1저자인 김준영 유니스트 생명과학부 박사는 “이번 연구에서 암 전이 과정 이해를 위해 처음으로 장기칩(Organ-on-a-Chip) 기술’을 적용했다”며 “이 칩은 간을 이루는 다양한 세포를 함께 배양해 사람의 간 조직과 비슷할 뿐 아니라 혈액도 흘려보낼 수 있어 혈액 속에 포함된 나노소포체의 역할을 제대로 이해할 수 있었다”고 말했다. 연구진은 또 간 전이가 잘 발생하는 췌장암 나노소포체도 유방암 나노소포체와 같은 효과를 보이는 것을 확인했다. 조 교수는 “유방암의 간 전이과정에 대한 이해를 바탕으로 간 전이 빈도가 높은 췌장암, 대장암 등의 전이 과정도 밝혀낼 수 있을 것”이라고 말했다. 조 교수는 “간은 전이암 발생빈도가 매우 높고, 전이 암 발생 시 사망률이 크게 늘어난다는 점을 고려하면 이번 연구의 의미가 크다”며 이번 발견이 암 전이를 조기 진단하거나 환자 맞춤형 진단·치료법을 개발하는 데 유용할 것으로 기대했다. 이번 연구는 아산병원의 이희진 교수팀과 함께 진행했다고 연구진은 밝혔다. 논문 제목은 `Three-Dimensional Human Liver-Chip Emulating Pre-Metastatic Niche Formation by Breast Cancer-Derived Extracellular Vesicles'. 곽노필 선임기자 nopil@hani.co.kr
항상 시민과 함께하겠습니다. 한겨레 구독신청 하기







![[사설] 노동자 안전 뒷전 중대재해법 후퇴가 민생 대책인가 [사설] 노동자 안전 뒷전 중대재해법 후퇴가 민생 대책인가](http://flexible.img.hani.co.kr/flexible/normal/300/180/imgdb/child/2024/0116/53_17053980971276_20240116503438.jpg)

![[올해의 책] 숙제를 풀 실마리를 찾아, 다시 책으로 ①국내서 [올해의 책] 숙제를 풀 실마리를 찾아, 다시 책으로 ①국내서](http://flexible.img.hani.co.kr/flexible/normal/800/320/imgdb/original/2023/1228/20231228503768.jpg)
![[올해의 책] 숙제를 풀 실마리를 찾아, 다시 책으로 ②번역서 [올해의 책] 숙제를 풀 실마리를 찾아, 다시 책으로 ②번역서](http://flexible.img.hani.co.kr/flexible/normal/500/300/imgdb/original/2023/1228/20231228503807.jpg)











